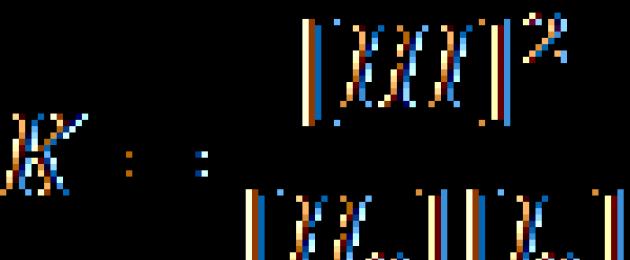Большинство химических реакций обратимы, т.е. протекают одновременно в противоположных направлениях. В тех случаях, когда прямая и обратная реакции идут с одинаковой скоростью, наступает химическое равновесие. Например, в обратимой гомогенной реакции: H 2 (г) + I 2 (г) ↔ 2HI(г) соотношение скоростей прямой и обратной реакций согласно закону действующих масс зависит от соотношения концентраций реагирующих веществ, а именно: скорость прямой реакции: υ 1 = k 1 [Н 2 ]. Скорость обратной реакции: υ 2 = k 2 2 .
Если H 2 и I 2 – исходные вещества, то в первый момент скорость прямой реакции определяется их начальными концентрациями, а скорость обратной реакции равна нулю. По мере израсходования H 2 и I 2 и образования HI скорость прямой реакции уменьшается, а скорость обратной реакции возрастает. Спустя некоторое время обе скорости уравниваются, и в системе устанавливается химическое равновесие, т.е. число образующихся и расходуемых молекул HI в единицу времени становится одинаковым.
Так как при химическом равновесии скорости прямой и обратной реакций равны V 1 = V 2 , то k 1 = k 2 2 .
Поскольку k 1 и k 2 при данной температуре постоянны, то их отношение будет постоянным. Обозначая его через K, получим:

К – называется константой химического равновесия, а приведенное уравнение – законом действующих масс (Гульдберга - Ваале).
В общем случае для реакции вида аА+bB+…↔dD+eE+… константа равновесия равна ![]() . Для взаимодействия между газообразными веществами часто пользуются выражением , в котором реагенты представлены равновесными парциальными давлениями p. Для упомянутой реакции
. Для взаимодействия между газообразными веществами часто пользуются выражением , в котором реагенты представлены равновесными парциальными давлениями p. Для упомянутой реакции  .
.
Состояние равновесия характеризует тот предел, до которого в данных условиях реакция протекает самопроизвольно (∆G<0). Если в системе наступило химическое равновесие, то дальнейшее изменение изобарного потенциала происходить не будет, т.е. ∆G=0.
Соотношение между равновесными концентрациями не зависит от того, какие вещества берутся в качестве исходных (например, H 2 и I 2 или HI), т.е. к состоянию равновесия можно подойти с обеих сторон.
Константа химического равновесия зависит от природы реагентов и от температуры; от давления (если оно слишком высокое) и от концентрации реагентов константа равновесия не зависит.
Влияние на константу равновесия температуры, энтальпийного и энтропийного факторов . Константа равновесия связана с изменением стандартного изобарно-изотермического потенциала химической реакции ∆G o простым уравнением ∆G o =-RT ln K.
Из него видно, что большим отрицательным значениям ∆G o (∆G o <<0) отвечают большие значения К, т.е. в равновесной смеси преобладают продукты взаимодействия. Если же ∆G o характеризуется большими положительными значениями (∆G o >>0), то в равновесной смеси преобладают исходные вещества. Указанное уравнение позволяет по величине ∆G o вычислить К, а затем и равновесные концентрации (парциальные давления) реагентов. Если учесть, что ∆G o =∆Н o -Т∆S o , то после некоторого преобразования получим ![]() . Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры. Влияние на константу равновесия природы реагентов определяет ее зависимость от энтальпийного и энтропийного факторов.
. Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры. Влияние на константу равновесия природы реагентов определяет ее зависимость от энтальпийного и энтропийного факторов.
Принцип Ле Шателье
Состояние химического равновесия сохраняется при данных неизменных условиях любое время. При изменении же условий состояние равновесия нарушается, так как при этом скорости противоположных процессов изменяются в разной степени. Однако спустя некоторое время система снова приходит в состояние равновесия, но уже отвечающее новым изменившимся условиям.
Смещение равновесия в зависимости от изменения условий в общем виде определяется принципом Ле-Шателье (или принципом подвижного равновесия): если на систему, находящуюся в равновесии, оказывать воздействие извне путем изменения какого-либо из условий, определяющих положение равновесия, то оно смещается в направлении того процесса, протекание которого ослабляет эффект произведенного воздействия.
Так, повышение температуры вызывает смещение равновесия в направлении того из процессов, течение которого сопровождается поглощением тепла, а понижение температуры действует в противоположном направлении. Подобно этому повышение давления смещает равновесие в направлении процесса, сопровождающегося уменьшением объема, а понижение давления действует в противоположную сторону. Например, в равновесной системе 3Н 2 +N 2 2H 3 N, ∆H o = -46,2 кДж повышение температуры усиливает разложение H 3 N на водород и азот, так как этот процесс эндотермический. Повышение давления смещает равновесие в сторону образования H 3 N, ибо при этом уменьшается объем.
Если в систему, находящуюся в состоянии равновесия, добавить некоторое количество какого-либо из веществ, участвующих в реакции (или наоборот, удалить из системы), то скорости прямой и обратной реакций изменяются, но постепенно снова уравниваются. Иными словами, система снова приходит к состоянию химического равновесия. В этом новом состоянии равновесные концентрации всех веществ, присутствующих в системе, будут отличаться от первоначальных равновесных концентраций, но соотношение между ними останется прежним. Таким образом, в системе, находящейся в состоянии равновесия, нельзя изменить концентрацию одного из веществ, не вызвав изменения концентраций всех остальных.
В соответствии с принципом Ле Шателье введение в равновесную систему дополнительных количеств какого-либо реагента вызывает сдвиг равновесия в том направлении, при котором концентрация этого вещества уменьшается и соответственно увеличивается концентрация продуктов его взаимодействия.
Изучение химического равновесия имеет большое значение как для теоретических исследований, так и для решения практических задач. Определяя положение равновесия для различных температур и давлений, можно выбрать наиболее благоприятные условия проведения химического процесса. При окончательном выборе условий проведения процесса учитывают также их влияние на скорость процесса.
Пример 1. Вычисление константы равновесия реакции по равновесным концентрациям реагирующих веществ.
Вычислите константу равновесия реакции А+В 2С, если равновесные концентрации [А]=0,3моль∙л -1 ; [В]=1,1моль∙л -1 ; [С]=2,1моль∙л -1 .
Решение. Выражение константы равновесия для данной реакции имеет вид: . Подставим сюда указанные в условии задачи равновесные концентрации: =5,79.
Пример 2 . Вычисление равновесных концентраций реагирующих веществ. Реакция протекает по уравнению А+2В С.
Определите равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В соответственно равны 0,5 и 0,7 моль∙л -1 , а константа равновесия реакции К р =50.
Решение. На каждый моль веществ А и В образуется 2 моль вещества С. Если понижение концентрации веществ А и В обозначить через Х моль, то увеличение концентрации вещества будет равно 2Х моль. Равновесные концентрации реагирующих веществ будут:
С А =(о,5-х)моль∙л -1 ; С В =(0,7-х)моль∙л -1 ; С С =2х моль∙л -1
х 1 =0,86; х 2 =0,44
По условию задачи справедливо значение х 2 . Отсюда равновесные концентрации реагирующих веществ равны:
С А =0,5-0,44=0,06моль∙л -1 ; С В =0,7-0,44=0,26моль∙л -1 ; С С =0,44∙2=0,88моль∙л -1 .
Пример 3. Определение изменения энергии Гиббса ∆G o реакции по значению константы равновесия К р. Рассчитайте энергию Гиббса и определите возможность протекания реакции СО+Cl 2 =COCl 2 при 700К, если константа равновесия равна Кр=1,0685∙10 -4 . Парциальное давление всех реагирующих веществ одинаково и равно 101325Па.
Решение.
∆G 700 =2,303∙RT ![]() .
.
Для данного процесса:
Так как ∆Gо<0, то реакция СО+Cl 2 COCl 2 при 700К возможна.
Пример 4 . Смещение химического равновесия. В каком направлении сместится равновесие в системе N 2 +3H 2 2NH 3 -22ккал:
а) при увеличении концентрации N 2 ;
б) при увеличении концентрации Н 2 ;
в) при повышении температуры;
г)при уменьшении давления?
Решение. Увеличение концентрации веществ, стоящих в левой части уравнения реакции, по правилу Ле-Шателье должно вызвать процесс, стремящийся ослабить оказанное воздействие, привести к уменьшению концентраций, т.е. равновесие сместится вправо (случаи а и б).
Реакция синтеза аммиака – экзотермическая. Повышение температуры вызывает смещение равновесия влево – в сторону эндотермической реакции, ослабляющей оказанное воздействие (случай в).
Уменьшение давления (случай г) будет благоприятствовать реакции, ведущей к увеличению объема системы, т.е. в сторону образования N 2 и Н 2 .
Пример 5. Во сколько раз изменится скорость прямой и обратной реакции в системе 2SO 2 (г) + О 2 (г) 2SO 3 (r) если объем газовой смеси уменьшится в три раза? В какую сторону сместится равновесие системы?
Решение. Обозначим концентрации реагирующих веществ: =а, =b, =с. Согласно закону действующих масс, скорости прямой и обратной реакций до изменения объема равны
v пр = Ка 2 b, v обр = К 1 с 2
После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза: = 3а, [О 2 ] = 3b; = 3с. При новых концентрациях скорости v" np прямой и обратной реакций:
v" np = K(3a) 2 (3b) = 27 Ka 2 b; v o 6 p = K 1 (3c) 2 = 9K 1 c 2 .
![]() ;
; ![]()
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной - только в девять раз. Равновесие системы сместилось в сторону образования SO 3 .
Пример 6. Вычислите, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70 0 С, если температурный коэффициент реакции равен 2.
Решение. Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант-Гоффа по формуле
Следовательно, скорость реакции при 70°С большескорости реакции при 30° С в 16 раз.
Пример 7. Константа равновесия гомогенной системы
СО(г) + Н 2 О(г) СО 2 (г) + Н 2 (г) при 850°С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации: [СО] ИСХ = 3 моль/л, [Н 2 О] ИСХ = 2 моль/л.
Решение. При равновесии скорости прямой и обратной реакций равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы:
V np = К 1 [СО][Н 2 О]; V o б p = К 2 [СО 2 ][Н 2 ];
![]()
В условии задачи даны исходные концентрации, тогда как в выражение К р входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация [СО 2 ] Р = х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По столько же молей (х моль/л) СО и Н 2 О расходуется для образования по х молей СО 2 и Н 2 . Следовательно, равновесные концентрации всех четырех веществ (моль/л):
[СО 2 ] Р = [Н 2 ] р = х; [СО] Р = (3 –х); P =(2-х).
Зная константу равновесия, находим значение х, а затем исходные концентрации всех веществ:
![]() ; х 2 =6-2х-3х + х 2
; 5х = 6, л = 1,2 моль/л.
; х 2 =6-2х-3х + х 2
; 5х = 6, л = 1,2 моль/л.
Рассмотрим обратную реакцию общего вида
Экспериментальные исследования показывают, что в состоянии равновесия выполняется следующее соотношение:

(квадратные скобки означают концентрацию). Приведенное соотношение представляет собой математическое выражение закона действующих масс, или закона химического равновесия, согласно которому в состоянии химического равновесия при определенной температуре произведение концентраций продуктов реакции в степенях, показатели
которых равны соответствующим коэффициентам в стехиометрическом уравнении реакции, деленное на аналогичное произведение концентраций реагентов в соответствующих степенях, представляет собой постоянную величину. Эта постоянная называется константой равновесия. Выражение константы равновесия через концентрации продуктов и реагентов характерно для реакций в растворах.
Отметим, что правая часть выражения для константы равновесия содержит только концентрации растворенных веществ. Она не должна включать никаких членов, относящихся к участвующим в реакции чистым твердым веществам, чистым жидкостям, растворителям, так как эти члены постоянны.
Для реакций с участием газов константа равновесия выражается через парциальные давления газов, а не через их концентрации. В этом случае константу равновесия обозначают символом .
Концентрацию газа можно выразить через его давление при помощи уравнения состояния идеального газа (см. разд. 3.1):
Из этого уравнения следует
где - концентрация газа, которую можно обозначить как [газ]. Поскольку -постоянная величина, можно записать, что при заданной температуре
Выразим константу равновесия для реакции между водородом и иодом через парциальные давления этих газов.
Уравнение указанной реакции имеет вид
Следовательно, константа равновесия этой реакции определяется выражением
![]()
Обратим внимание на то, что концентрации или парциальные давления продуктов, т. е. веществ, указанных в правой части химического уравнения, всегда образуют числитель, а концентрации или парциальные давления реагентов, т. е. веществ, указанных в левой части химического уравнения, всегда образуют знаменатель выражения для константы равновесия.
Единицы измерения для константы равновесия
Константа равновесия может оказаться размерной или безразмерной величиной в зависимости от вида ее математического выражения. В приведенном выше примере константа равновесия является безразмерной величиной, поскольку числитель и знаменатель дроби имеют одинаковые размерности. В противном случае константа равновесия имеет размерность, выражаемую в единицах концентрации или давления.
Какова размерность константы равновесия для следующей реакции?
Следовательно, она имеет размерность (моль-дм-3)

Итак, размерность рассматриваемой константы равновесия или дм3/моль.
Какую размерность имеет константа равновесия для следующей реакции?

Константа равновесия указанной реакции определяется выражением
Следовательно, она имеет размерность
![]()

Итак, размерность данной константы равновесия: атм или Па.
Гетерогенные равновесия
До сих пор мы приводили примеры только гомогенных равновесий. Например, в реакции синтеза иодоводорода и продукт, и оба реагента находятся в газообразном состоянии.
В качестве примера реакции, приводящей к гетерогенному равновесию, рассмотрим термическую диссоциацию карбоната кальция
Константа равновесия этой реакции определяется выражением
![]()
Отметим, что в это выражение не входят никакие члены, относящиеся к двум твердым веществам, участвующим в реакции. В приведенном примере константа равновесия представляет собой давление диссоциации карбоната кальция. Она показывает, что если карбонат кальция нагревают в закрытом сосуде, то его давление диссоциации при фиксированной температуре не зависит от количества карбоната кальция. В следующем разделе мы узнаем, каким образом константа равновесия изменяется в зависимости от температуры. В рассматриваемом примере давление диссоциации превышает 1 атм лишь при температуре выше Поэтому для того, чтобы диоксид
Концентрационная константа
При расчетах равновесий в реальных системах необходимо учитывать присутствие посторонних веществ и их влияние на поведение исходных веществ и продуктов изучаемой реакции. Это влияние может выразиться и в электростатическом взаимодействии ионов, и в химическом взаимодействии с образованием малодиссоциированных или малорастворимых продуктов. В обоих случаях наблюдается сдвиг равновесия изучаемой реакции. Концентрационная константа выражается через общие концентрации, а не активности исходных веществ и продуктов реакции. В том случае, когда посторонние вещества не вступают в конкурирующие химические реакции, концентрационную константу можно выразить через равновесные концентрации. Для удобства изучения часто концентрационную константу, выраженную через равновесные концентрации, называют реальной константой, а концентрационную константу, выраженную через общие концентрации, – условной константой.
Состояние равновесия характеризуется реальной (концентрационной) константой
если отличия от идеальности обусловлены только электростатическими взаимодействиями А, В, С и D с посторонними ионами.
Активность и равновесная концентрация любого иона функционально связаны между собой простым соотношением. Например, для иона А
a A = γ A [A]
Коэффициент пропорциональности γ , называемый коэффициентом активности, характеризует степень отклонения системы от идеальной из-за электростатических взаимодействий ионов, участвующих в изучаемой реакции, с посторонними (или собственными, если их концентрация высока) ионами. В идеальной системе a A = [А] и коэффициент активности равен единице. Это означает, что электростатические взаимодействия отсутствуют.
Величина коэффициента активности зависит от заряда и ионной силы, создаваемой всеми ионами в растворе:
Здесь I – ионная сила; [i] – равновесная концентрация иона; z i - его заряд.
Коэффициенты активности индивидуальных ионов можно теоретически оценить по формулам Дебая - Хюккеля
Если I < 0.01 (1-3)
Если I < 0.1 (1-4)
Здесь А и В – константы, зависящие от температуры и диэлектрической проницаемости растворителя (для воды при 20°С А = 0.5 и B = 0.3); а – расстояние максимального сближения ионов; эти величины обычно приводятся в справочных таблицах. Поскольку колебания в значениях а не слишком сказываются на конечном результате, рекомендуется брать постоянное значение a = 3 А. Следовательно,
Коэффициент активности индивидуального иона нельзя измерить экспериментально, так как нельзя получить раствор, содержащий только положительные или только отрицательные ионы.
Для электролита A m B n экспериментально можно определить лишь средний коэффициент активности, который связан с коэффициентами активности индивидуальных ионов γ A и γ B соотношениями:
для бинарного электролита АВ
для электролита типа A m B n
Средний коэффициент активности можно рассчитать и теоретически, используя формулы Дебая - Хюккеля
Если I < 0.01
Если I < 0.1
Здесь а, А и В имеют те же значения, что и в формулах (1-3) и (1-4), поэтому
При низких ионных силах (I < 0.1) величины средних коэффициентов активности, рассчитанные по формулам Дебая - Хюккеля и найденные экспериментально, удовлетворительно совпадают. Это говорит о правомочности использования в этих условиях формул (1-3) - (1-4) для расчета величин γ ± и активности электролитов. Эти же формулы используются и для расчета коэффициентов активности индивидуальных ионов, хотя правильность таких расчетов нельзя проверить экспериментально.
Для более точного расчета коэффициентов активности предложено вводить в формулы Дебая - Хюккеля дополнительные члены. Например, уравнение Дэвиса позволяет вычислить коэффициенты активности электролитов и индивидуальных ионов для ионных сил 0.2 - 0.5 с погрешностью, не превышающей 10%. Уравнение Дэвиса для коэффициента активности индивидуального иона имеет вид:
а для среднего коэффициента активности электролита А m В n:
Величины коэффициентов активности индивидуальных ионов при различных ионных силах и средние коэффициенты активности для растворов электролитов разной концентрации, рассчитанные по формулам Дебая - Хюккеля, приводятся в справочниках.
Зная коэффициенты активности, можно оценить активность иона или электролита в растворе. Для облегчения расчетов можно пользоваться следующими допущениями:
1. Коэффициенты активности ионов одинакового заряда независимо от радиуса ионов примерно равны. Поэтому в справочниках иногда приводятся усредненные величины коэффициентов активности для одно-, двух-, трех- и четырех-зарядных ионов.
2. Коэффициенты активности нейтральных частиц в разбавленных растворах электролитов полагают равными единице.
3. Очень разбавленные растворы электролитов, например насыщенный раствор малорастворимого электролита, можно считать идеальными.
Часто при расчетах сложных равновесий коэффициенты активности принимают равными единице. Такое допущение оправдано по ряду причин. Во-первых, величины коэффициентов активности, найденные по формулам Дебая - Хюккеля, могут в этих случаях оказаться очень далекими от истинных. Во-вторых, влияние химических факторов на равновесие гораздо больше, чем электростатических сил, поэтому пренебрежение последними при расчетах сложных равновесий не вносит ощутимую погрешность в результаты.
Материал из Википедии - свободной энциклопедии
Конста́нта равнове́сия - величина, определяющая для данной химической реакции соотношение между термодинамическими активностями (либо, в зависимости от условий протекания реакции, парциальными давлениями , концентрациями или фугитивностями) исходных веществ и продуктов в состоянии химического равновесия (в соответствии с законом действующих масс). Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.
Способы выражения константы равновесия
Например, для реакции окисления монооксида углерода :
2CO + O 2 = 2CO 2
константа равновесия может быть рассчитана по уравнению:
где Δn - изменение числа молей веществ в ходе реакции. Видно, что K x зависит от давления. Если число молей продуктов реакции равно числу молей исходных веществ (), то .
Стандартная константа равновесия
Стандартная константа равновесия реакции в смеси идеальных газов (когда начальные парциальные давления участников реакции равны их значениям в стандартном состоянии = 0,1013 МПа или 1 атм) может быть рассчитана по выражению:
где - относительные парциальные давления компонентов, .
Стандартная константа равновесия - безразмерная величина. Она связана с K p соотношением:
Видно, что если выражены в атмосферах, то и .
Для реакции в смеси реальных газов в стандартном начальном состоянии парциальные фугитивности газов принимаются равными их парциальным давлениям = 0,1013 МПа или 1 атм. K f связана с K 0 соотношением:
где γ i - коэффициент фугитивности i-го реального газа в смеси.
Константа равновесия реакций в гетерогенных системах
FeO т + CO г = Fe т + CO 2гконстанта равновесия (при условии, что газовая фаза идеальна) имеет вид:
Термодинамическое описание равновесия
Наряду с обозначением Q для соотношения активностей веществ в произвольный момент реакции t ("коэффициент реакции ")
(обозначения для приведённой ниже реакции; последнее равенство написано в обозначении, что стехиометрические коэффициент берутся со знаком "+" для продуктов и со знаком "-" для исходных веществ)
в химической термодинамике используется обозначение K eq для такого же по форме соотношения между равновесными активностями веществ
(то есть соотношения активностей в момент , в момент равновесия). Далее приведено термодинамическое описание химического равновесия и описана связь K eq со стандартной энергией Гиббса процесса.
В системе, где протекает химическая реакция
равновесие может быть описано условием
где есть химическая переменная
или, то же самое условие равновесия может быть записано с использованием химических потенциалов как
где химические потенциалы
здесь {A} - строго говоря, активность реагента A; при допущениях об идеальных газах можно заменить их на давления, для реальных газов можно заменить на фугитивности , при допущении о том, что раствор подчиняется закону Генри , можно заменить на мольные доли , и при допущении, что раствор подчиняется закону Рауля - на парциальные давления ; для системы в равновесии может быть заменена на равновесную молярную концентрацию или на равновесную активность.
Равновесный состав смеси и направление реакции
Упомянутый выше "коэффициент реакции" Q (другие обозначения, встречающиеся в литературе - или , "произведение реакции")
отражает соотношение текущих активностей всех участников реакции и может быть использован для определения направления реакции в момент, для которого известен Q
Если в момент t коэффициент Q > K, то текущие активности продуктов больше равновесных, и значит они должны уменьшиться к тому моменту, когда установится равновесие, то есть в данный момент протекает обратная реакция; Если Q = K, то равновесное состояние достигнуто и скорости прямой и обратной реакций равны; Если Q < K, то
С использованием величины записывается уравнение изотермы химической реакции
Где - стехиометрические коэффициенты (для продуктов - со знаком "+", для исходных веществ - со знаком "-"; так же, как и в выражениях для Q и K), а - химические потенциалы а стандартная энергия Гиббса и стандартная константа суть
Где - стандартные химические потенциалы
Уравнение изотермы показывает, как величина Q связана с изменением свободной энергии реакции:
При для прямой реакции , то есть для продуктов прямой реакции больше, чем для исходных веществ - это означает, что прямая реакция запрещена (значит, не запрещена обратная); при для прямой реакции , то есть реакция достигла равновесного состояния; при для прямой реакции , то есть эта самопроизвольное протекание этой реакции разрешено
Величина по определению имеет смысл только для состояния равновесия, то есть для состояния с и . Величина ничего не говорит о скоростях реакций, но она описывает состав системы в состоянии равновесия.
Если K >> 1, то в системе преобладают продукты (прямой) реакции Если K << 1, то в системе преобладают исходные вещества (продукты обратной реакции)
Стандартные состояния
Стандартная энергия Гиббса реакции в газовой смеси - энергия Гиббса реакции при стандартных парциальных давлениях всех компонентов, равных 0,1013 МПа (1 атм). Стандартная энергия Гиббса реакции в растворе - энергия Гиббса при стандартном состоянии раствора, за которое принимают гипотетический раствор со свойствами предельно разбавленного раствора , но с концентрацией всех реагентов, равной единице. Для чистого вещества и жидкости стандартная энергия Гиббса совпадает с энергией Гиббса образования этих веществ. Величина стандартной энергии Гиббса реакции может быть использована для приближенной оценки термодинамической возможности протекания реакции в данном направлении, если начальные условия не сильно отличаются от стандартных. Кроме того, сравнивая величины стандартной энергии Гиббса нескольких реакций, можно выбрать наиболее предпочтительные, для которых имеет наибольшую по модулю отрицательную величину.
Кинетическое описание
Для обратимой химической реакции константа равновесия K eq может быть выражена через константы скорости прямых и обратных реакций. Рассмотрим элементарную обратимую химическую реакцию первого порядка
По определению, равновесие задаётся условием , то есть равенством скоростей прямой и обратной реакций.
В соответствии с законом действующих масс
Где k - константа скорости соответствующей реакции, а - равновесные активности реагентов этой реакции, возведённые в степени, равные их стехиометрическим коэффициентам
можно записать условие равновесия в виде
(см. термодинамическое описание константы равновесия), что возможно только если
Это важное соотношение даёт одну из «точек соприкосновения» химической кинетики и химической термодинамики .
Множественные равновесия
В случае, когда в системе устанавливается сразу несколько равновесий (то есть одновременного или последовательного протекает нескольких процессов), каждый из них может быть охарактеризован своей константой равновесия, из которых можно выразить общую константу равновесия для всей совокупности процессов. Можно рассмотреть такую ситуацию на примере ступенчатой диссоциации двухосновной кислоты H 2 A. Водный раствор её будет содержать частицы (сольватированные) H + , H 2 A, HA - and A 2- . Процесс диссоциации протекает в две ступени:
K 1 и K 2 - константы первой и второй ступеней диссоциации соответственно. Из них можно выразить "полную" константу равновесия, для процесса полной диссоциации :
Другой пример множественного равновесия - анализ системы осадок /растворимое комплексное соединение . Допустим, имеется равновесие
Реакцию можно представить в виде двух последовательных равновесий - равновесия разложения комплексного иона на составляющие его ионы, которое характеризуется "константой нестойкости" (величина, обратная "константе устойчивости" β):
и равновесия перехода ионов из объёма растворителя в кристаллическую решётку
с учётом того, что для твёрдых веществ активность принимается равной 1 , а в разбавленных растворах активности могут быть заменены на молярные концентрации, получаем
Тогда суммарное равновесие будет описываться константой
И значение этой константы будет условием преобладания в равновесной смеси комплексного соединения или твёрдой соли: как и выше, если K << 1, то в равновесной смеси большая часть ионов связана в комплексное соединение, если K >> 1, то в равновесном состоянии в системе большая часть ионов связана в кристаллической фазе.
Зависимость константы равновесия от температуры
Зависимость константы равновесия реакции от температуры может быть описана уравнением изобары химической реакции (изобары Вант-Гоффа):
Методы расчета константы равновесия
Расчётные методы определения константы равновесия реакции обычно сводятся к вычислению тем или иным способом стандартного изменения энергии Гиббса в ходе реакции (ΔG 0 ), а затем использованию формулы:
, где - универсальная газовая постоянная .
При этом следует помнить, что энергия Гиббса - функция состояния системы, то есть она не зависит от пути процесса, от механизма реакции, а определяется лишь начальным и конечным состояниями системы. Следовательно, если непосредственное определение или расчёт ΔG 0 для некоторой реакции по каким-либо причинам затруднены, можно подобрать такие промежуточные реакции, для которых ΔG 0 известно или может быть легко определено, и суммирование которых даст рассматриваемую реакцию (см. Закон Гесса). В частности, в качестве таких промежуточных реакций часто используют реакции образования соединений из элементов.
Энтропийный расчёт изменения энергии Гиббса и константы равновесия реакции
Энтропийный метод расчёта ΔG реакции является одним из самых распространённых и удобных . Он основан на соотношении:
или, соответственно, для стандартного изменения энергии Гиббса:
Здесь ΔH 0 при постоянных давлении и температуре равно тепловому эффекту реакции, методы расчёта и экспериментального определения которого известны - см., например, уравнение Кирхгофа :
Необходимо получить изменение энтропии в ходе реакции. Эта задача может быть решена несколькими способами, например:
- По термическим данным - с опорой на тепловую теорему Нернста и с использованием сведений о температурной зависимости теплоёмкости участников реакции. Например, для веществ, при нормальных условиях находящихся в твёрдом состоянии:
Итак, если известны , и температурные зависимости теплоёмкости, может быть рассчитано по формуле:
Несколько упрощённый вариант этой формулы получают, считая сумму теплоёмкостей веществ не зависящей от температуры и равной сумме теплоёмкостей при 298 K:
И еще более упрощённый расчёт проводят, приравнивая сумму теплоёмкостей к нулю:
Переход от к константе равновесия осуществляется по приведённой выше формуле.
Расчёт константы равновесия методами статистической термодинамики
Экспериментальное определение константы равновесия
См. также
Напишите отзыв о статье "Константа равновесия"
Примечания
Литература
- Киреев В.А. Методы практических расчётов в термодинамике химических реакций. - 2-е изд. - М ., 1975.
- Жоров Ю.М. Термодинамика химических процессов. - М ., 1985.
Отрывок, характеризующий Константа равновесия
И, отделавшись от молодого человека, не умеющего жить, она возвратилась к своим занятиям хозяйки дома и продолжала прислушиваться и приглядываться, готовая подать помощь на тот пункт, где ослабевал разговор. Как хозяин прядильной мастерской, посадив работников по местам, прохаживается по заведению, замечая неподвижность или непривычный, скрипящий, слишком громкий звук веретена, торопливо идет, сдерживает или пускает его в надлежащий ход, так и Анна Павловна, прохаживаясь по своей гостиной, подходила к замолкнувшему или слишком много говорившему кружку и одним словом или перемещением опять заводила равномерную, приличную разговорную машину. Но среди этих забот всё виден был в ней особенный страх за Пьера. Она заботливо поглядывала на него в то время, как он подошел послушать то, что говорилось около Мортемара, и отошел к другому кружку, где говорил аббат. Для Пьера, воспитанного за границей, этот вечер Анны Павловны был первый, который он видел в России. Он знал, что тут собрана вся интеллигенция Петербурга, и у него, как у ребенка в игрушечной лавке, разбегались глаза. Он всё боялся пропустить умные разговоры, которые он может услыхать. Глядя на уверенные и изящные выражения лиц, собранных здесь, он всё ждал чего нибудь особенно умного. Наконец, он подошел к Морио. Разговор показался ему интересен, и он остановился, ожидая случая высказать свои мысли, как это любят молодые люди.Вечер Анны Павловны был пущен. Веретена с разных сторон равномерно и не умолкая шумели. Кроме ma tante, около которой сидела только одна пожилая дама с исплаканным, худым лицом, несколько чужая в этом блестящем обществе, общество разбилось на три кружка. В одном, более мужском, центром был аббат; в другом, молодом, красавица княжна Элен, дочь князя Василия, и хорошенькая, румяная, слишком полная по своей молодости, маленькая княгиня Болконская. В третьем Мортемар и Анна Павловна.
Виконт был миловидный, с мягкими чертами и приемами, молодой человек, очевидно считавший себя знаменитостью, но, по благовоспитанности, скромно предоставлявший пользоваться собой тому обществу, в котором он находился. Анна Павловна, очевидно, угощала им своих гостей. Как хороший метрд`отель подает как нечто сверхъестественно прекрасное тот кусок говядины, который есть не захочется, если увидать его в грязной кухне, так в нынешний вечер Анна Павловна сервировала своим гостям сначала виконта, потом аббата, как что то сверхъестественно утонченное. В кружке Мортемара заговорили тотчас об убиении герцога Энгиенского. Виконт сказал, что герцог Энгиенский погиб от своего великодушия, и что были особенные причины озлобления Бонапарта.
– Ah! voyons. Contez nous cela, vicomte, [Расскажите нам это, виконт,] – сказала Анна Павловна, с радостью чувствуя, как чем то a la Louis XV [в стиле Людовика XV] отзывалась эта фраза, – contez nous cela, vicomte.
Виконт поклонился в знак покорности и учтиво улыбнулся. Анна Павловна сделала круг около виконта и пригласила всех слушать его рассказ.
– Le vicomte a ete personnellement connu de monseigneur, [Виконт был лично знаком с герцогом,] – шепнула Анна Павловна одному. – Le vicomte est un parfait conteur , – проговорила она другому. – Comme on voit l"homme de la bonne compagnie [Как сейчас виден человек хорошего общества], – сказала она третьему; и виконт был подан обществу в самом изящном и выгодном для него свете, как ростбиф на горячем блюде, посыпанный зеленью.
Виконт хотел уже начать свой рассказ и тонко улыбнулся.
– Переходите сюда, chere Helene, [милая Элен,] – сказала Анна Павловна красавице княжне, которая сидела поодаль, составляя центр другого кружка.
Княжна Элен улыбалась; она поднялась с тою же неизменяющеюся улыбкой вполне красивой женщины, с которою она вошла в гостиную. Слегка шумя своею белою бальною робой, убранною плющем и мохом, и блестя белизною плеч, глянцем волос и брильянтов, она прошла между расступившимися мужчинами и прямо, не глядя ни на кого, но всем улыбаясь и как бы любезно предоставляя каждому право любоваться красотою своего стана, полных плеч, очень открытой, по тогдашней моде, груди и спины, и как будто внося с собою блеск бала, подошла к Анне Павловне. Элен была так хороша, что не только не было в ней заметно и тени кокетства, но, напротив, ей как будто совестно было за свою несомненную и слишком сильно и победительно действующую красоту. Она как будто желала и не могла умалить действие своей красоты. Quelle belle personne! [Какая красавица!] – говорил каждый, кто ее видел.
Как будто пораженный чем то необычайным, виконт пожал плечами и о опустил глаза в то время, как она усаживалась перед ним и освещала и его всё тою же неизменною улыбкой.
– Madame, je crains pour mes moyens devant un pareil auditoire, [Я, право, опасаюсь за свои способности перед такой публикой,] сказал он, наклоняя с улыбкой голову.
Княжна облокотила свою открытую полную руку на столик и не нашла нужным что либо сказать. Она улыбаясь ждала. Во все время рассказа она сидела прямо, посматривая изредка то на свою полную красивую руку, которая от давления на стол изменила свою форму, то на еще более красивую грудь, на которой она поправляла брильянтовое ожерелье; поправляла несколько раз складки своего платья и, когда рассказ производил впечатление, оглядывалась на Анну Павловну и тотчас же принимала то самое выражение, которое было на лице фрейлины, и потом опять успокоивалась в сияющей улыбке. Вслед за Элен перешла и маленькая княгиня от чайного стола.
– Attendez moi, je vais prendre mon ouvrage, [Подождите, я возьму мою работу,] – проговорила она. – Voyons, a quoi pensez vous? – обратилась она к князю Ипполиту: – apportez moi mon ridicule. [О чем вы думаете? Принесите мой ридикюль.]
Княгиня, улыбаясь и говоря со всеми, вдруг произвела перестановку и, усевшись, весело оправилась.
– Теперь мне хорошо, – приговаривала она и, попросив начинать, принялась за работу.
Князь Ипполит перенес ей ридикюль, перешел за нею и, близко придвинув к ней кресло, сел подле нее.
Le charmant Hippolyte [Очаровательный Ипполит] поражал своим необыкновенным сходством с сестрою красавицей и еще более тем, что, несмотря на сходство, он был поразительно дурен собой. Черты его лица были те же, как и у сестры, но у той все освещалось жизнерадостною, самодовольною, молодою, неизменною улыбкой жизни и необычайною, античною красотой тела; у брата, напротив, то же лицо было отуманено идиотизмом и неизменно выражало самоуверенную брюзгливость, а тело было худощаво и слабо. Глаза, нос, рот – все сжималось как будто в одну неопределенную и скучную гримасу, а руки и ноги всегда принимали неестественное положение.
– Ce n"est pas une histoire de revenants? [Это не история о привидениях?] – сказал он, усевшись подле княгини и торопливо пристроив к глазам свой лорнет, как будто без этого инструмента он не мог начать говорить.
– Mais non, mon cher, [Вовсе нет,] – пожимая плечами, сказал удивленный рассказчик.
– C"est que je deteste les histoires de revenants, [Дело в том, что я терпеть не могу историй о привидениях,] – сказал он таким тоном, что видно было, – он сказал эти слова, а потом уже понял, что они значили.
Из за самоуверенности, с которой он говорил, никто не мог понять, очень ли умно или очень глупо то, что он сказал. Он был в темнозеленом фраке, в панталонах цвета cuisse de nymphe effrayee, [бедра испуганной нимфы,] как он сам говорил, в чулках и башмаках.
Vicomte [Виконт] рассказал очень мило о том ходившем тогда анекдоте, что герцог Энгиенский тайно ездил в Париж для свидания с m lle George, [мадмуазель Жорж,] и что там он встретился с Бонапарте, пользовавшимся тоже милостями знаменитой актрисы, и что там, встретившись с герцогом, Наполеон случайно упал в тот обморок, которому он был подвержен, и находился во власти герцога, которой герцог не воспользовался, но что Бонапарте впоследствии за это то великодушие и отмстил смертью герцогу.
Рассказ был очень мил и интересен, особенно в том месте, где соперники вдруг узнают друг друга, и дамы, казалось, были в волнении.
– Charmant, [Очаровательно,] – сказала Анна Павловна, оглядываясь вопросительно на маленькую княгиню.
– Charmant, – прошептала маленькая княгиня, втыкая иголку в работу, как будто в знак того, что интерес и прелесть рассказа мешают ей продолжать работу.
Виконт оценил эту молчаливую похвалу и, благодарно улыбнувшись, стал продолжать; но в это время Анна Павловна, все поглядывавшая на страшного для нее молодого человека, заметила, что он что то слишком горячо и громко говорит с аббатом, и поспешила на помощь к опасному месту. Действительно, Пьеру удалось завязать с аббатом разговор о политическом равновесии, и аббат, видимо заинтересованный простодушной горячностью молодого человека, развивал перед ним свою любимую идею. Оба слишком оживленно и естественно слушали и говорили, и это то не понравилось Анне Павловне.
– Средство – Европейское равновесие и droit des gens [международное право], – говорил аббат. – Стоит одному могущественному государству, как Россия, прославленному за варварство, стать бескорыстно во главе союза, имеющего целью равновесие Европы, – и она спасет мир!
– Как же вы найдете такое равновесие? – начал было Пьер; но в это время подошла Анна Павловна и, строго взглянув на Пьера, спросила итальянца о том, как он переносит здешний климат. Лицо итальянца вдруг изменилось и приняло оскорбительно притворно сладкое выражение, которое, видимо, было привычно ему в разговоре с женщинами.
– Я так очарован прелестями ума и образования общества, в особенности женского, в которое я имел счастье быть принят, что не успел еще подумать о климате, – сказал он.
Не выпуская уже аббата и Пьера, Анна Павловна для удобства наблюдения присоединила их к общему кружку.
В это время в гостиную вошло новое лицо. Новое лицо это был молодой князь Андрей Болконский, муж маленькой княгини. Князь Болконский был небольшого роста, весьма красивый молодой человек с определенными и сухими чертами. Всё в его фигуре, начиная от усталого, скучающего взгляда до тихого мерного шага, представляло самую резкую противоположность с его маленькою, оживленною женой. Ему, видимо, все бывшие в гостиной не только были знакомы, но уж надоели ему так, что и смотреть на них и слушать их ему было очень скучно. Из всех же прискучивших ему лиц, лицо его хорошенькой жены, казалось, больше всех ему надоело. С гримасой, портившею его красивое лицо, он отвернулся от нее. Он поцеловал руку Анны Павловны и, щурясь, оглядел всё общество.
– Vous vous enrolez pour la guerre, mon prince? [Вы собираетесь на войну, князь?] – сказала Анна Павловна.
– Le general Koutouzoff, – сказал Болконский, ударяя на последнем слоге zoff , как француз, – a bien voulu de moi pour aide de camp… [Генералу Кутузову угодно меня к себе в адъютанты.]
– Et Lise, votre femme? [А Лиза, ваша жена?]
– Она поедет в деревню.
– Как вам не грех лишать нас вашей прелестной жены?
– Andre, [Андрей,] – сказала его жена, обращаясь к мужу тем же кокетливым тоном, каким она обращалась к посторонним, – какую историю нам рассказал виконт о m lle Жорж и Бонапарте!
Князь Андрей зажмурился и отвернулся. Пьер, со времени входа князя Андрея в гостиную не спускавший с него радостных, дружелюбных глаз, подошел к нему и взял его за руку. Князь Андрей, не оглядываясь, морщил лицо в гримасу, выражавшую досаду на того, кто трогает его за руку, но, увидав улыбающееся лицо Пьера, улыбнулся неожиданно доброй и приятной улыбкой.
– Вот как!… И ты в большом свете! – сказал он Пьеру.
– Я знал, что вы будете, – отвечал Пьер. – Я приеду к вам ужинать, – прибавил он тихо, чтобы не мешать виконту, который продолжал свой рассказ. – Можно?
– Нет, нельзя, – сказал князь Андрей смеясь, пожатием руки давая знать Пьеру, что этого не нужно спрашивать.
Он что то хотел сказать еще, но в это время поднялся князь Василий с дочерью, и два молодых человека встали, чтобы дать им дорогу.
– Вы меня извините, мой милый виконт, – сказал князь Василий французу, ласково притягивая его за рукав вниз к стулу, чтоб он не вставал. – Этот несчастный праздник у посланника лишает меня удовольствия и прерывает вас. Очень мне грустно покидать ваш восхитительный вечер, – сказал он Анне Павловне.
Дочь его, княжна Элен, слегка придерживая складки платья, пошла между стульев, и улыбка сияла еще светлее на ее прекрасном лице. Пьер смотрел почти испуганными, восторженными глазами на эту красавицу, когда она проходила мимо него.
– Очень хороша, – сказал князь Андрей.
– Очень, – сказал Пьер.
Проходя мимо, князь Василий схватил Пьера за руку и обратился к Анне Павловне.
– Образуйте мне этого медведя, – сказал он. – Вот он месяц живет у меня, и в первый раз я его вижу в свете. Ничто так не нужно молодому человеку, как общество умных женщин.
Анна Павловна улыбнулась и обещалась заняться Пьером, который, она знала, приходился родня по отцу князю Василью. Пожилая дама, сидевшая прежде с ma tante, торопливо встала и догнала князя Василья в передней. С лица ее исчезла вся прежняя притворность интереса. Доброе, исплаканное лицо ее выражало только беспокойство и страх.
– Что же вы мне скажете, князь, о моем Борисе? – сказала она, догоняя его в передней. (Она выговаривала имя Борис с особенным ударением на о). – Я не могу оставаться дольше в Петербурге. Скажите, какие известия я могу привезти моему бедному мальчику?
Несмотря на то, что князь Василий неохотно и почти неучтиво слушал пожилую даму и даже выказывал нетерпение, она ласково и трогательно улыбалась ему и, чтоб он не ушел, взяла его за руку.
– Что вам стоит сказать слово государю, и он прямо будет переведен в гвардию, – просила она.
– Поверьте, что я сделаю всё, что могу, княгиня, – отвечал князь Василий, – но мне трудно просить государя; я бы советовал вам обратиться к Румянцеву, через князя Голицына: это было бы умнее.
Пожилая дама носила имя княгини Друбецкой, одной из лучших фамилий России, но она была бедна, давно вышла из света и утратила прежние связи. Она приехала теперь, чтобы выхлопотать определение в гвардию своему единственному сыну. Только затем, чтоб увидеть князя Василия, она назвалась и приехала на вечер к Анне Павловне, только затем она слушала историю виконта. Она испугалась слов князя Василия; когда то красивое лицо ее выразило озлобление, но это продолжалось только минуту. Она опять улыбнулась и крепче схватила за руку князя Василия.
– Послушайте, князь, – сказала она, – я никогда не просила вас, никогда не буду просить, никогда не напоминала вам о дружбе моего отца к вам. Но теперь, я Богом заклинаю вас, сделайте это для моего сына, и я буду считать вас благодетелем, – торопливо прибавила она. – Нет, вы не сердитесь, а вы обещайте мне. Я просила Голицына, он отказал. Soyez le bon enfant que vous аvez ete, [Будьте добрым малым, как вы были,] – говорила она, стараясь улыбаться, тогда как в ее глазах были слезы.
– Папа, мы опоздаем, – сказала, повернув свою красивую голову на античных плечах, княжна Элен, ожидавшая у двери.
Но влияние в свете есть капитал, который надо беречь, чтоб он не исчез. Князь Василий знал это, и, раз сообразив, что ежели бы он стал просить за всех, кто его просит, то вскоре ему нельзя было бы просить за себя, он редко употреблял свое влияние. В деле княгини Друбецкой он почувствовал, однако, после ее нового призыва, что то вроде укора совести. Она напомнила ему правду: первыми шагами своими в службе он был обязан ее отцу. Кроме того, он видел по ее приемам, что она – одна из тех женщин, особенно матерей, которые, однажды взяв себе что нибудь в голову, не отстанут до тех пор, пока не исполнят их желания, а в противном случае готовы на ежедневные, ежеминутные приставания и даже на сцены. Это последнее соображение поколебало его.
– Chere Анна Михайловна, – сказал он с своею всегдашнею фамильярностью и скукой в голосе, – для меня почти невозможно сделать то, что вы хотите; но чтобы доказать вам, как я люблю вас и чту память покойного отца вашего, я сделаю невозможное: сын ваш будет переведен в гвардию, вот вам моя рука. Довольны вы?
– Милый мой, вы благодетель! Я иного и не ждала от вас; я знала, как вы добры.
Он хотел уйти.
– Постойте, два слова. Une fois passe aux gardes… [Раз он перейдет в гвардию…] – Она замялась: – Вы хороши с Михаилом Иларионовичем Кутузовым, рекомендуйте ему Бориса в адъютанты. Тогда бы я была покойна, и тогда бы уж…
Князь Василий улыбнулся.
– Этого не обещаю. Вы не знаете, как осаждают Кутузова с тех пор, как он назначен главнокомандующим. Он мне сам говорил, что все московские барыни сговорились отдать ему всех своих детей в адъютанты.
– Нет, обещайте, я не пущу вас, милый, благодетель мой…
– Папа! – опять тем же тоном повторила красавица, – мы опоздаем.
– Ну, au revoir, [до свиданья,] прощайте. Видите?
– Так завтра вы доложите государю?
– Непременно, а Кутузову не обещаю.
– Нет, обещайте, обещайте, Basile, [Василий,] – сказала вслед ему Анна Михайловна, с улыбкой молодой кокетки, которая когда то, должно быть, была ей свойственна, а теперь так не шла к ее истощенному лицу.
Она, видимо, забыла свои годы и пускала в ход, по привычке, все старинные женские средства. Но как только он вышел, лицо ее опять приняло то же холодное, притворное выражение, которое было на нем прежде. Она вернулась к кружку, в котором виконт продолжал рассказывать, и опять сделала вид, что слушает, дожидаясь времени уехать, так как дело ее было сделано.
– Но как вы находите всю эту последнюю комедию du sacre de Milan? [миланского помазания?] – сказала Анна Павловна. Et la nouvelle comedie des peuples de Genes et de Lucques, qui viennent presenter leurs voeux a M. Buonaparte assis sur un trone, et exaucant les voeux des nations! Adorable! Non, mais c"est a en devenir folle! On dirait, que le monde entier a perdu la tete. [И вот новая комедия: народы Генуи и Лукки изъявляют свои желания господину Бонапарте. И господин Бонапарте сидит на троне и исполняет желания народов. 0! это восхитительно! Нет, от этого можно с ума сойти. Подумаешь, что весь свет потерял голову.]
Князь Андрей усмехнулся, прямо глядя в лицо Анны Павловны.
– «Dieu me la donne, gare a qui la touche», – сказал он (слова Бонапарте, сказанные при возложении короны). – On dit qu"il a ete tres beau en prononcant ces paroles, [Бог мне дал корону. Беда тому, кто ее тронет. – Говорят, он был очень хорош, произнося эти слова,] – прибавил он и еще раз повторил эти слова по итальянски: «Dio mi la dona, guai a chi la tocca».
– J"espere enfin, – продолжала Анна Павловна, – que ca a ete la goutte d"eau qui fera deborder le verre. Les souverains ne peuvent plus supporter cet homme, qui menace tout. [Надеюсь, что это была, наконец, та капля, которая переполнит стакан. Государи не могут более терпеть этого человека, который угрожает всему.]
Количественная характеристика, показывающая направление реакции и смещение концентрации веществ, называется константой равновесия химической реакции. Константа равновесия зависит от температуры и природы реагентов.
Обратимые и необратимые реакции
Все реакции можно разделить на два типа:
- обратимые , одновременно протекающие в двух взаимно противоположных направлениях;
- необратимые , протекающие в одном направлении с полным расходом хотя бы одного исходного вещества.
При необратимых реакциях обычно образуются нерастворимые вещества в виде осадка или газа. К таким реакциям относятся:
- горение:
C 2 H 5 OH + 3O 2 → 2CO 2 + H 2 O;
- разложение:
2KMnO 4 → K 2 MnO 4 + MnO 2 + H 2 O;
- присоединение с образованием осадка или газа:
BaCl 2 + Na 2 SO 4 → BaSO 4 ↓ + 2NaCl.

Рис. 1. Образование осадка BaSO 4 .
Обратимые реакции возможны только в определённых неизменных условиях. Исходные вещества дают новое вещество, которое тут же распадается на составные части и собирается вновь. Например, в результате реакции 2NO + O 2 ↔ 2NO 2 оксид азота (IV) легко разлагается на оксид азота (II) и кислород.
Равновесие
Через определённое время скорость обратимой реакции замедляется. Достигается химическое равновесие - состояние, при котором не происходит изменения концентрации исходных веществ и продуктов реакции с течением времени, так как скорость прямой и обратной реакций уравниваются. Равновесие возможно только в гомогенных системах, то есть все реагирующие вещества являются либо жидкостями, либо газами.
Рассмотрим химическое равновесие на примере реакции взаимодействия водорода с йодом:
- прямая реакция -
H 2 + I 2 ↔ 2HI;
- обратная реакция -
2HI ↔ H 2 + I 2 .
Как только смешиваются два реагента - водород и йод - йодоводорода ещё не существует, так как простые вещества только вступают в реакцию. Большое количество исходных веществ активно реагируют друг с другом, поэтому скорость прямой реакции будет максимальной. При этом обратная реакция не протекает, и скорость её равна нулю.
Скорость прямой реакции можно выразить графически:
ν пр = k пр ∙ ∙ ,
где k пр - константа скорости прямой реакции.
Со временем реагенты расходуются, их концентрация снижается. Соответственно, скорость прямой реакции уменьшается. Одновременно с этим увеличивается концентрация нового вещества - йодоводорода. При накоплении он начинает разлагаться, и скорость обратной реакции повышается. Её можно выразить как
ν обр = k обр ∙ 2 .
Йодоводород в квадрате, так как коэффициент молекулы равен двум.
В определённый момент скорости прямой и обратной реакции уравниваются. Наступает состояние химического равновесия.

Рис. 2. График зависимости скорости реакции от времени.
Равновесие можно сместить либо в сторону исходных веществ, либо в сторону продуктов реакции. Смещение под воздействием внешних факторов называется принципом Ле Шателье. На равновесие влияют температура, давление, концентрация одного из веществ.
Расчёт константы
В состоянии равновесия обе реакции идут, но при этом концентрации веществ находятся в равновесии (образуются равновесные концентрации), так как уравновешенны скорости (ν пр = ν обр).
Химическое равновесие характеризуется константой химического равновесия, которая выражается сводной формулой:
K p = k пр / k обр = const.
Константы скорости реакции можно выразить через соотношение скорости реакции. Возьмём условное уравнение обратной реакции:
aA + bB ↔ cC + dD.
Тогда скорости прямой и обратной реакции будут равны:
- ν пр = k пр ∙ [A] p a ∙ [B] p b
- ν обр = k обр ∙ [C] p c ∙ [D] p d .
Соответственно, если
ν пр = ν обр,
k пр ∙ [A] p a ∙ [B] p b = k обр ∙ [C] p c ∙ [D] p d .
Отсюда можно выразить соотношение констант:
k обр / k пр = [C] p c ∙ [D] p d / [A] p a ∙ [B] p b .
Это соотношение равно константе равновесия:
K p = [C] p c ∙ [D] p d / [A] p a ∙ [B] p b .

Рис. 3. Формула константы равновесия.
Величина показывает, во сколько раз скорость прямой реакции больше скорости обратной реакции.
Что мы узнали?
Реакции в зависимости от конечных продуктов классифицируются на обратимые и необратимые. Обратимые реакции протекают в обе стороны: исходные вещества образуют конечные продукты, которые разлагаются на исходные вещества. В ходе реакции скорости прямой и обратной реакций уравновешиваются. Такое состояние называется химическим равновесием. Оно может быть выражено как соотношение произведения равновесных концентраций продуктов реакции к произведению разновесных концентраций исходных веществ.
Тест по теме
Оценка доклада
Средняя оценка: 4.8 . Всего получено оценок: 193.